🔥 Produits recommandés : Canon EOS R6 II • DJI Mini 4 Pro • MacBook Pro M4

Juin est le mois de la sensibilisation à la maladie d’Alzheimer et au cerveau. On pourrait dire que la sensibilisation aux troubles neurodégénératifs comme la maladie d’Alzheimer et la maladie de Parkinson – qui détruisent progressivement les cellules du cerveau avec l’âge – est déjà à son comble. Qui d’entre nous n’a pas encore été personnellement touché par ces voleurs d’intellect et de dignité ?
Devenue une épidémie mondiale, la maladie d’Alzheimer touche déjà près de six millions d’Américains et 50 millions de personnes dans le monde.
La maladie de Parkinson, deuxième maladie neurodégénérative la plus répandue, touche environ un million de personnes aux États-Unis et jusqu’à 10 millions dans le monde.
Une plus grande prise de conscience est-elle vraiment la solution ? On nous dit qu’il n’y a pas de bons traitements pour ces fléaux et que les facteurs de risque sont des choses sur lesquelles nous ne pouvons rien : notre âge, nos antécédents familiaux et les gènes que nous possédons. Le désespoir et l’impuissance s’ensuivent inévitablement, tandis que nous attendons passivement de voir qui sera le prochain à être frappé.
Dans la plupart des cas, ces troubles sont considérés comme « sporadiques » (aléatoires) et « idiopathiques » (d’origine mystérieuse). Bien que les causes sous-jacentes restent très incertaines, ces deux diagnostics se caractérisent par des anomalies microscopiques révélatrices qui constituent des cibles tentantes pour les chercheurs à l’esprit pharmaceutique.
Dans le cas de la maladie d’Alzheimer, les cibles médicamenteuses les plus populaires ont été les fameuses plaques bêta-amyloïdes et les enchevêtrements neurofibrillaires.
Dans le cas de la maladie de Parkinson, la protéine potentiellement toxique du jour est l’alpha-synucléine, une molécule nécessaire au fonctionnement normal des synapses cérébrales. Dans la grande majorité des cas de maladie de Parkinson, cette protéine s’agglomère en « fibrilles toxiques » mal repliées qui s’accumulent à l’intérieur de structures anormales appelées corps de Lewy.
Malheureusement, d’innombrables dollars de désespoir ont alimenté des décennies de recherche sophistiquée sur les médicaments, en s’attaquant à ces facteurs et à d’autres coupables potentiels, ce qui a conduit à exactement zéro médicament susceptible de faire une différence significative dans l’évolution de ces conditions jusqu’à présent.
Pourtant, l’espoir existe… si nous savons où le chercher. Et si les particularités visuelles telles que les plaques, les enchevêtrements et les corps de Lewy n’étaient pas les vrais méchants de l’histoire ? Dans la quête des véritables causes profondes, ces fragments pathologiques tentants pourraient-ils égarer les scientifiques curieux ? Dans le cas de la maladie de Parkinson, un tout nouvelarticle publié cette semaine par un groupe international de neuroscientifiques européens affirme que l’alpha-synucléine n’est rien d’autre qu’un leurre – un spectateur innocent qui n’apparaît coupable que par association.
Au lieu de nous laisser distraire par les objets brillants sous le microscope, nous ferions probablement mieux de prendre du recul et de regarder la situation dans son ensemble pour nous réorienter.
Aussi différentes qu’elles puissent paraître, ces maladies ont de nombreux points communs qui méritent notre attention. Le plus important est de loin celui que nous devons garder à l’esprit :
Les cellules cérébrales meurent
Dans la maladie d’Alzheimer, qui détruit progressivement l’ensemble du cerveau, ce sont les cellules de l’hippocampe, le centre de la mémoire du cerveau, qui sont parmi les premières à disparaître.
Dans la maladie de Parkinson, la mort et la destruction semblent commencer par les cellules productrices de dopamine de la substantia nigra, lecentre de coordination des mouvements du cerveau. Au fur et à mesure que ces précieuses cellules disparaissent, les symptômes classiques de dysfonctionnement moteur apparaissent : tremblements, rigidité, bradykinésie (ralentissement des mouvements) et modifications de l’élocution et de la démarche. Bien que les symptômes de la maladie de Parkinson puissent être atténués par un médicament appelé L-dopa, que le cerveau peut utiliser pour produire davantage de dopamine, aucun médicament n’a encore été mis au point pour ralentir ou arrêter la progression de cette maladie débilitante.
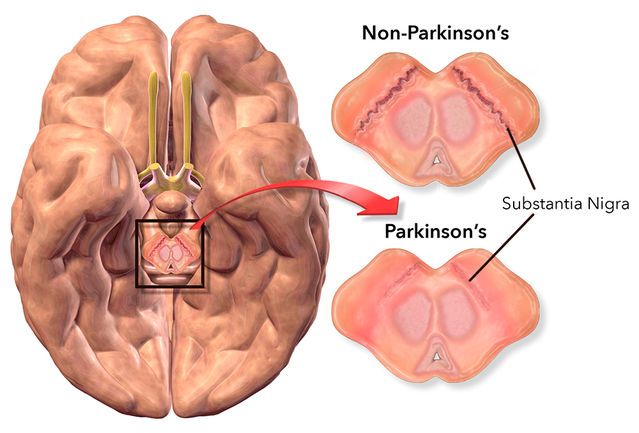
Pourquoi les cellules cérébrales meurent-elles ?
Devons-nous simplement accepter qu’il est normal et naturel pour un grand nombre d’entre nous de commencer à perdre aléatoirement des cellules dans l’hippocampe et/ou la substantia nigra avec l’âge ? Si nous comprenions ce qui les tue, nous pourrions peut-être faire quelque chose.
De multiples sources de données de qualité ont établi de manière convaincante que la résistance à l’insuline (ou prédiabète) est l’un des principaux moteurs de la plupart des cas de maladie d’Alzheimer, ce qui a conduit certains à qualifier la maladie d’Alzheimer de « diabète de type 3« . (Pour en savoir plus, lisez mon article de Psychology Today intitulé « Avoiding Alzheimer’s Disease Could Be Easier than You Think » (Éviter la maladie d’Alzheimer pourrait être plus facile que vous ne le pensez).
La majorité des Américains présentent aujourd’hui une résistance à l’insuline, un problème métabolique qui peut entraîner des taux d’insuline trop élevés dans le sang, en particulier en réponse aux glucides présents dans l’alimentation.
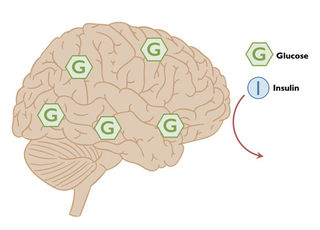
Chez les personnes souffrant de résistance à l’insuline, le glucose (sucre dans le sang) continue d’entrer dans le cerveau sans poser de questions ; c’est l’insuline qui peine à franchir la barrière hémato-encéphalique. Comme les cellules cérébrales ne peuvent pas transformer le glucose en énergie sans une quantité suffisante d’insuline, les personnes souffrant de résistance à l’insuline sont confrontées à une crise de l’énergie cérébrale.
Si vous êtes résistant à l’insuline, vos cellules cérébrales peuvent nager dans une mer de glucose et pourtant mourir de faim.
La maladie de Parkinson en tant que trouble métabolique
En tant que psychiatre ayant une expérience clinique dans le traitement des personnes atteintes de la maladie d’Alzheimer, j’écris et je parle de la maladie d’Alzheimer depuis un certain temps déjà, mais ce n’est que lorsque j’ai été invité à faire une présentation sur la résistance à l’insuline et les maladies neurodégénératives lors de la première conférence annuelle Keto-Live à Bergün, en Suisse, au début du mois, que je me suis plongé pour la première fois dans la recherche sur la maladie de Parkinson. Ce que j’ai découvert, c’est une multitude de similitudes métaboliques frappantes entre la maladie de Parkinson et la maladie d’Alzheimer :
- Problèmes d’utilisation du glucose dans le cerveau
- Dysfonctionnement mitochondrial
- Mauvais comportement des protéines
- Augmentation de l’apoptose ( suicide cellulaire)
- Inflammation
- Toxicité du glutamate
- Dommages oxydatifs
- Ralentissement de la conduction des cellules cérébrales
- Formation de produits de glycation avancée (AGE)
Il se trouve qu’un faible taux d’insuline dans le cerveau peut entraîner les quatre premiers phénomènes énumérés ci-dessus, tandis que les cinq derniers peuvent être provoqués par un taux élevé de glucose dans le cerveau. Cela suggère que, comme la maladie d’Alzheimer, la maladie de Parkinson pourrait être intimement liée à la résistance du cerveau à l’insuline .
Par exemple, tout comme la résistance à l’insuline contribue à expliquer l’accumulation de plaques et d’écheveaux dans le cerveau des personnes atteintes de la maladie d’Alzheimer, elle contribue également à expliquer la formation des corps de Lewy qui se cachent dans la grande majorité des cerveaux des personnes atteintes de la maladie de Parkinson. En effet, l’insuline active l’enzyme responsable d’empêcher l’alpha-synucléine de former les fibrilles toxiques que l’on trouve dans les corps de Lewy.
Combien de personnes atteintes de la maladie de Parkinson présentent une résistance à l’insuline ?
Une étude réalisée en 2018 à l’hôpital Cedars-Sinai de Los Angeles sur 154 patients non diabétiques atteints de la maladie de Parkinson a révélé que 58 % d’entre eux présentaient une résistance à l’insuline. Toutes ces personnes avaient une glycémie à jeun normale et, dans de nombreux cas, un taux d’hémoglobine A1C normal, ainsi qu’un poids corporel normal. En fait, un pourcentage surprenant de 42 % des personnes de poids normal atteintes de la maladie de Parkinson présentaient une résistance à l’insuline [déterminée par un indice HOMA de 2,0 ou plus et/ou un taux d’hémoglobine A1C de 5,7 ou plus]. Ces données soulignent le fait que les tests de diabète de routine et les mesures du poids corporel échouent souvent à détecter la résistance à l’insuline, trompant les gens en leur faisant croire qu’ils sont métaboliquement sains et qu’ils n’ont pas besoin de changer de mode de vie.
D’autres études ont montré que les personnes atteintes de la maladie de Parkinson qui présentent également une résistance à l’insuline sont plus susceptibles de présenter des symptômes graves, une progression plus rapide de la maladie et une démence liée à la maladie de Parkinson.
Ainsi, si la résistance à l’insuline n’est certainement pas le seul acteur du développement de la maladie de Parkinson, elle est clairement une force avec laquelle il faut compter dans la majorité des cas.
Emplacement, emplacement, emplacement
Si la résistance à l’insuline est un problème métabolique général qui affecte les niveaux de glucose et d’insuline de l’ensemble du cerveau, comment se fait-il que la maladie de Parkinson semble trouver son origine dans la substantia nigra ?
La substantia nigra demande beaucoup plus d’énergie que la plupart des autres régions du cerveau. Cela s’explique par le fait qu’elle est densément peuplée de neurones producteurs de dopamine fortement interconnectés, dont beaucoup sont mal isolés, voire totalement dépourvus d’isolation. La myéline, la substance blanche qui enveloppe les cellules nerveuses et rend la conduction électrique plus efficace, est largement absente dans cette région du cerveau, ce qui signifie que ces cellules utilisent plus d’énergie pour envoyer leurs messages électriques. Ces cellules possèdent également des propriétés de pacemaker qui contribuent à leur soif d’énergie. Ensemble, ces caractéristiques rendent les neurones dopaminergiques extrêmement vulnérables aux déficits énergétiques du cerveau causés par la résistance à l’insuline.
En fait, un article récemment publié soulève la possibilité fascinante que le problème le plus précoce et le plus fondamental sous-jacent à la fois à la maladie d’Alzheimer et à la maladie de Parkinson pourrait être la perte de neurones produisant de la dopamine dans l’ensemble du cerveau. Seules trois zones du cerveau synthétisent la dopamine : la substantia nigra (coordination des mouvements), le locus coeruleus (attention, éveil, réponse au stress) et l’aire tegmentale ventrale(émotion, cognition, motivation, plaisir). Cette hypothèse d’un déficit en dopamine peut contribuer à expliquer pourquoi il est si fréquent que les patients atteints de la maladie d’Alzheimer et de la maladie de Parkinson présentent des symptômes psychiatriques tels que des problèmes d’attention, d’humeur et de motivation, même à un stade relativement précoce de la maladie.
Il semblerait que tout ce que nous pourrions faire pour préserver les neurones exposés et gourmands en énergie de notre circuit dopaminergique serait une très bonne idée.
Les régimes cétogènes pour la maladie de Parkinson
Si, dans de nombreux cas, la maladie de Parkinson est en partie due à une crise énergétique au cours de laquelle le cerveau à faible teneur en insuline a du mal à traiter le glucose, il devrait être utile de fournir au cerveau une autre source de carburant.
Heureusement, les cétones constituent une excellente source de carburant pour la plupart des cellules cérébrales, et elles brûlent parfaitement dans un environnement à faible taux d’insuline. L’organisme génère naturellement des cétones à partir des graisses lorsque le taux d’insuline dans le sang est suffisamment bas pour que l’organisme passe en mode de combustion des graisses. Les régimes cétogènes, c’est-à-dire les régimes à très faible teneur en glucides, abaissent les taux de glucose et d’insuline dans le sang au point de produire des corps cétoniques mesurables dans la circulation sanguine.
Jusqu’à présent, il n’y a eu que deux études cliniques humaines sur les régimes cétogènes dans la maladie de Parkinson, mais les résultats semblent prometteurs.
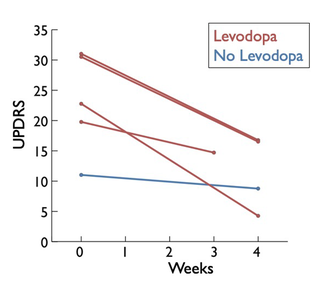
La première était une petite étude pilote réalisée en 2005 sur cinq patients en surpoids à qui l’on avait demandé de suivre un régime composé de 90 % de graisses, 8 % de protéines et 2 % de glucides. Tous les patients ont atteint la cétose, avec des niveaux de cétone dans le sang allant de 1,13 mM à 8,0 mM. Tous les patients ont perdu du poids et ont connu une réduction des symptômes mesurés par l’échelle d’évaluation unifiée de la maladie de Parkinson (Unified Parkinson’s Disease Rating Scale). La principale critique de cette étude est que quatre des cinq patients prenaient de la L-dopa, qui pénètre plus facilement dans le cerveau dans des conditions de faible teneur en protéines. Il est donc possible que les améliorations cliniques observées soient dues à une meilleure administration du médicament au cerveau plutôt qu’à la cétose, puisque ce régime de recherche particulier était conçu pour être relativement pauvre en protéines.
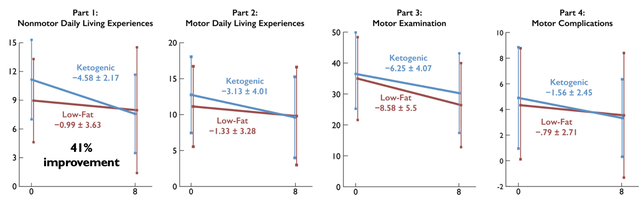
La seconde étude est un essai randomisé réalisé en 2018 auprès de 38 personnes atteintes de la maladie de Parkinson, qui a comparé un régime pauvre en graisses à un régime cétogène pendant huit semaines. Les deux régimes étaient conçus pour contenir suffisamment (plutôt que peu) de protéines (75 g/jour) et le même nombre de calories (1 750/jour). Le régime pauvre en graisses contenait 42 grammes de graisses et 246 grammes de glucides par jour. Le régime cétogène contenait 152 grammes de graisses et 16 grammes de glucides par jour. Les personnes du groupe cétogène ont atteint des niveaux de cétone dans le sang de 1,15 ± 0,59 mM.
Les deux groupes ont montré des améliorations légères mais significatives des symptômes moteurs et non moteurs ; cependant, le groupe cétogène a montré des améliorations beaucoup plus importantes (41 pour cent) des symptômes non moteurs. Ce résultat est important, car les symptômes non moteurs, tels que les problèmes urinaires, la douleur, la fatigue, la somnolence diurne et les troubles cognitifs, sont parmi les moins susceptibles de répondre à la L-dopa.
Réveillez-vous et sentez l’insuline
Tout comme la maladie d’Alzheimer ne survient pas du jour au lendemain, la maladie de Parkinson commence bien avant l’apparition des symptômes. Lorsqu’une personne remarque les symptômes de la maladie de Parkinson, au moins 50 % des neurones produisant de la dopamine dans la substantia nigra ont déjà été détruits.
Heureusement, vous n’avez pas à rester les bras croisés pendant que votre cerveau se détériore tranquillement de l’intérieur. La résistance à l’insuline est un facteur de risque majeur de cette maladie dévastatrice, contre lequel vous pouvez agir immédiatement.
Beaucoup de mes patients pensent que la meilleure façon d’augmenter l’énergie du cerveau est de manger plus de glucides. Bien que cela semble logique, la vérité paradoxale est que plus vous mangez de sucre, plus votre cerveau devient résistant à l’insuline, ce qui rend de plus en plus difficile la transformation du sucre en énergie par les cellules cérébrales.
Si vous découvrez que vous souffrez d’une résistance à l’insuline, vous pouvez dès maintenant prendre des mesures pour abaisser votre taux d’insuline et réduire le risque de maladies neurodégénératives. Pour en savoir plus sur la façon de déterminer si vous souffrez de résistance à l’insuline, d’améliorer votre métabolisme et de protéger votre système de signalisation de l’insuline à l’aide de stratégies simples liées au mode de vie, consultez mon article intitulé « Comment diagnostiquer, prévenir et traiter la résistance à l’insuline« , qui comprend un PDF téléchargeable (gratuit) de tests simples de résistance à l’insuline que vous pouvez apporter lors de votre prochaine visite médicale, ainsi qu’une infographie sur les moyens de manger plus sainement que vous pouvez utiliser dès maintenant pour améliorer votre métabolisme.
Il est courant que les campagnes de sensibilisation sollicitent des dons pour la recherche, dont la plupart sont axés sur les médicaments, qui ont tous échoué. La sensibilisation au lien important entre la santé métabolique et les maladies neurodégénératives pourrait inspirer des recherches indispensables sur la nutrition et le mode de vie et, dans le même temps, donner aux individus les moyens d’investir dans des changements de mode de vie qui pourraient changer le cours de leur avenir.



